من المعلوم أنه عند وضع جسمين عند درجات حرارة مختلفة بينهما اتصال حراري فإن الحرارة تنتقل من الجسم الأعلى درجة حرارة إلى الجسم الأقل درجة حرارة، ويسمى هذا تدفق حراري heat flow ويستمر حتى يصل الجسمين إلى نفس درجة الحرارة وعندها يكونا في حالة اتزان حراري Thermal Equilibrium.
حاول العلماء تفسير ظاهرة التدفق الحراري بافتراض جسيمات غير مرئية تدعى الكلوريك Caloric، تعمل على نقل الحرارة بين الأجسام. ولكن كان هذا الافتراض غير صحيح حيث لا يمكن تفسير العديد من الظواهر الحرارية مثل عدم تغير درجة الحرارة عند حالة التحول من الحالة السائلة إلى الحالة الغازية مثل غليان الماء، ولكن العالم جول Joule اثبت بالتجربة العملية أن التدفق الحراري ما هو إلا انتقال للطاقة وأن الحرارة صورة من صور الطاقة.
The word of ” heat flow” is an energy transfer that take place as a consequence of temperature difference only.
أي أن التدفق الحراري هو انتقال الطاقة الناتج عن اختلاف درجات الحرارة.
ودرجة الحرارة ما هي إلا مقياس للطاقة الداخلية للمادة وكلما زادت درجة الحرارة زادت الطاقة الداخلية أي زادت الطاقة الحركية لجزيئاته.
The unit of heat is ”calorie” which is defined as the amount of heat (energy) required to raise the temperature of 1g of water from 14.5oC to 15oC.
وبعد أن اثبت العالم جول أن الحرارة هي طاقة فيمكن التعبير عن وحدة الحرارة بالجول وقد اثبت عملياً أن:
1cal = 4.186J or 1J = 0.2389cal
The mechanical equivalent of heat
قام العالم جول بتصميم التجربة الموضحة في الشكل التالي والتي اثبت فيها أن الطاقة الميكانيكية تتحول إلى حرارة وان الحرارة ما هي إلا صورة من صور الطاقة ويمكن تحويلها من صورة إلى أخرى.
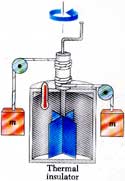
تعتمد التجربة على قياس التغير في طاقة الوضع للأثقال التي تحرك المروحة داخل الإناء المعزول والتي ينتج عنها ارتفاع في درجة الحرارة، وبدراسة التغير في طاقة الوضع mgh مع ارتفاع درجة حرارة الماء في الإناء يمكن إيجاد علاقة تناسب طردي بينهما ووجد أن ثابت التناسب..
The proportionality constant = 4.186 J/Kg.Co
Therefore 1cal = 4.186J
السعة الحرارية والسعة الحرارية النوعية Heat capacity and specific heat
The heat capacity is defined as the amount of heat energy needed to raise the temperature of a sample by 1 degree celsius.
Therefore the quantity of heat added to a substance is equal to the change in temperature
Q = C DT
The heat capacity of any object is proportional to its mass.
![]()
where c is called the specific heat.
يوضح الجدول التالي السعة الحرارية لبعض المواد عند درجة حرارة 25 درجة مئوية وعند الضغط الجوي.
| Al | 900J/kg.Co | wood | 1700J/kg.Co | |
| Cu | 387J/kg.Co | glass | 837J/kg.Co | |
| Ag | 129J/kg.Co | water | 4186J/kg.Co | |
| Pb | 128J/kg.Co | ice | 2090J/kg.Co |
نلاحظ أن الماء له اكبر سعة حرارية نوعية بحيث أنه يلزم 4186 جول لرفع درجة حرارة 1 كيلوجرام من الماء درجة مئوية واحدة بينما يلزم 900 جول من الحرارة للألمنيوم.
we can now express the heat energy Q transferred between a substance of mass m and its surrounding for a temperature change Tf-Ti=DT as
Q = m c DT
من هذه المعادلة يتضح أنه عندما تكتسب المادة حرارة فإن كلا من كمية الحرارة والتغير في درجة الحرارة يكون موجباً، وعندما تفقد المادة حرارة فإن التغير في درجة الحرارة يكون بالسالب وتكون كمية الحرارة سالبة.
Example
A 0.05kg of metal is heated to 200oC and then dropped into a beaker containing 0.4kg of water initially at 20oC. If the final equilibrium temperature of the mixed system is 22.4oC find the specific heat of the metal. What is the total heat transferred to water in cooling the metal?
Solution
يعتبر هذا المثال بمثابة تجربة عملية لتعيين السعة الحرارية للمواد وهنا قمنا بتسخين المعدن إلى درجة حرارة 200 درجة مئوية وأسقطت في كمية من الماء ذات كتلة محددة عند درجة حرارة 20 درجة مئوية ولتصبح درجة حرارة المعدن والماء 22.4 درجة مئوية. وبالتالي فإن الحرارة المفقودة بواسطة المعدن تساوي الحرارة المكتسبة بواسطة الماء.
Heat lost by the metal = heat gained by water
mx cx (Ti-Tf) = mw cw (Tf-Ti)
(0.05Kg) cx (200oC-22.4oC) = (0.4kg)(4186J/kg.Co)(22.4oC-20oC)
cx = 453J/kg.Co
(b) Q = m c (Ti-Tf) = 0.05 ´ 453 ´ (200-22.4) = 4020J
Example
A man fires a silver bullet of mass 2g with a velocity of 200m/sec into a wall. What is the temperature change of the bullet?
Solution
تكتسب الرصاصة طاقة حركة تتحول إلى حرارة عند اصطدامها بالجدار وبهذا يتضح أن الحرارة صورة من صور الطاقة.
The kinetic energy of the bullet Ek = 1/2 m v2 = 40J
Q = m c DT
where c for silver is 234Jkg.Co
DT = Q/mc = 85.5Co
الحرارة الكامنة Latent heat
وجدنا في الموضوع السابق أنه عند التسخين أي تزويد المادة بحرارة فإن القانون السابق Q = m c DT يشير إلى أن هناك تغير موجب في درجة الحرارة او تغير سالب إذا فقد الجسم حرارة، أي انه دائما يكون هناك تغيير في درجة الحرارة مع الانتقال الحراري ولكن هذا ليس صحيحاً في جميع الحالات حيث أن درجة الحرارة تثبت عندما تتحول حالة المادة من صورة إلى إلى أخرى مثل الماء إلى بخار الماء حيث تثبت درجة الحرارة عند 100 درجة مئوية عند الضغط الجوي وتسمى درجة الغليان. وهذا يعني أن كمية الحرارة التي يكتسبها الجسم لا تزيد من درجة حرارته بل تقوم على تحويل حالته Phase change.
Solid º Liquid melting
Liquid º gas boiling
The heat or energy required to change the phase of a given mass m of a substance is given by
Q = m L
where L is called the latent heat (hidden heat) of substance
Note that there are two latent heat for any substance on for the melting called latent heat of fusion Lf (Solid º Liquid) and the other is for the boiling called the latent heat of vaporization Lv (Liquid º gas)
Always Lv > Lf
وذلك لأن الشغل اللازم لتحويل السائل إلى غاز (المسافة بين جزيئات الغاز أكثر تباعداً من السائل) أكبر من الشغل اللازم لتحويل الصلب إلى سائل حيث المسافة بين جزيئات الصلب والسائل متقاربة.
ملاحظة:
عند التعامل مع مسائل من هذا النوع يجب الانتباه إلى درجات الحرارة المعطاة في المسألة لأن الحل يعتمد على هل المادة مرت في تغير في حالتها أم لا.
Example
What is the heat required to convert a 1g of ice at -30oC to steam at 120oC? where cice=2090J/kg.Co, Cw=4286J/kg.Co, Csteam=2000J/kg.Co, Lf=333000J/kg, and Lv=2260000J/kg.
Solution
لإيجاد كمية الحرارة المطلوبة لتحويل الثلج إلى ماء ومن ثم إلى بخار يلزم أن نحسب أولا كمية الحرارة اللازمة لرفع درجة الثلج من -30 إلى صفر ثم نحسب كمية الحرارة اللازمة لتحول الثلج إلى ماء عند درجة صفر، ثم حساب كمية الحرارة اللازمة لرفع درجة حرارة الماء من صفر إلى 100 درجة، ثم نحسب كمية الحرارة اللازمة لتحويل الماء إلى بخار عند درجة حرارة 100, ثم كمية الحرارة اللازمة لرفع درجة البخار من 100 إلى 120 درجة. الشكل التالي يوضح العلاقة بين كمية الحرارة ودرجة الحرارة.
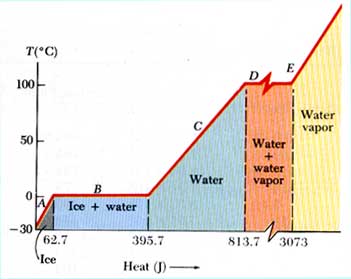
Part A ice from -30oC to 0oC
Q = mice cice DT = 62.7J
Part B ice to water + ice at 0oC
Q = m Lf = 333J
Part C water from 0oC to 100oC
Q = mw cw DT = 419J
Part D water to water + steam at 100oC
Q = m Lv = 2260J
Part E steam from 100oC to 120oC
Q = msteam csteam DT = 40.2J
The total energy = 62.7 + 333 + 419 + 2260 + 40.2 = 3110J
Problem
What mass of steam initially at 130oC is needed to warm 200g of water in a 100g glass container from 20oC to 50oC?


