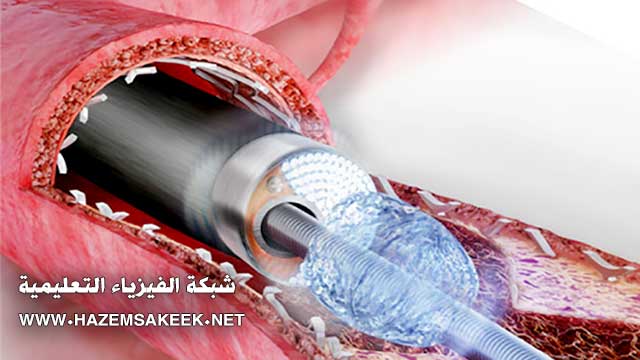
 ليزر الاكسيمر له خصائص مميزة تجعله مناسب للاستخدام في التخلص من انسداد الشرايين وdebulk atheromatous. ولكي نفهم تأثيرها على نظام الشرايين، فانه من المهم ان نفهم بعض أساسيات فيزياء الليزر. كلمة LASER هي اختصار Light Amplification by Stimulated Emission of Radiation أي تكبير الضوء بواسطة الانبعاث المستحث للإشعاع.. وبالطبع هناك الكثير من أنواع الليزرات التي تصنف حسب الطول الموجي للضوء المنبعث، وكذلك الطاقة التي يمتلكها الشعاع، وإذا ما كان هذا الشعاع يعمل بنظام النبضات مثل ضوء الفلاش أو انه شعاع مستمر مثل ضوء المصباح العادي.
ليزر الاكسيمر له خصائص مميزة تجعله مناسب للاستخدام في التخلص من انسداد الشرايين وdebulk atheromatous. ولكي نفهم تأثيرها على نظام الشرايين، فانه من المهم ان نفهم بعض أساسيات فيزياء الليزر. كلمة LASER هي اختصار Light Amplification by Stimulated Emission of Radiation أي تكبير الضوء بواسطة الانبعاث المستحث للإشعاع.. وبالطبع هناك الكثير من أنواع الليزرات التي تصنف حسب الطول الموجي للضوء المنبعث، وكذلك الطاقة التي يمتلكها الشعاع، وإذا ما كان هذا الشعاع يعمل بنظام النبضات مثل ضوء الفلاش أو انه شعاع مستمر مثل ضوء المصباح العادي.
وفعالية أي ليزر لتطبيقات علاج انسداد الشرايين يعتمد على كيف يتفاعل الضوء مع الأغشية الحية داخل الشرايين.
المبدأ الأساسي لعمل الليزر في معالجة تصلب الشرايين هو ان يتم تطبيق طاقة الليزر مباشرة على الانسدادات داخل الشرايين، وبالتالي يتم التخلص من الانسداد بدون إصابة محيط الشريان نفسه. ويعتبر الليزر وسيلة عملية يمكن استخدامها في علاج انسداد الأوعية الدموية حيث ان الليزر عبارة عن شعاع ضوئي أحادي اللون يمكن نقله عبر أنبوبة رفيعة من الألياف الضوئية (قسطر) إلى الأغشية الحية بدقة عالية جدا. وأول متغير يمكن تعريفه في حالة التفاعل بين ضوء الليزر والأغشية الحية هو الطول الموجي. حيث ان كل نوع من أنواع الليزر يكون له طول موجي محدد بواسطة مادة الوسط المستخدم في الليزر (الشكل 1).
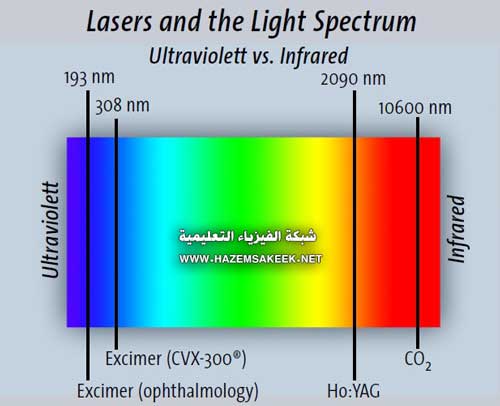
الشكل 1 الليزر والطيف الكهرومغناطيسي
المتغير الأكثر أهمية في تحديد التأثير البيولوجي لتأثير الضوء على الأغشية الحية هو عمق الاختراق للشعاع في الأغشية، أو كم مقدار العمق الذي يتمكن شعاع الليزر من الانتشار داخل الأغشية. هذا المتغير، يعرف بعمق الامتصاص absorption depth، أو المسافة التي يمتص فيها شعاع الليزر بمقدار 37% أي (1/e) من قيمته الأصلية خلال الأغشية، وهذا يحدد فقط بالطول الموجي ونوع الأغشية. ومن اجل عمل دقيق، فان عمق الاختراق يجب ان يكون اصغر ما يمكن، وذلك لنضمن ان التأثير يكون موضعيا في النقطة التي يطبق فيها الشعاع.
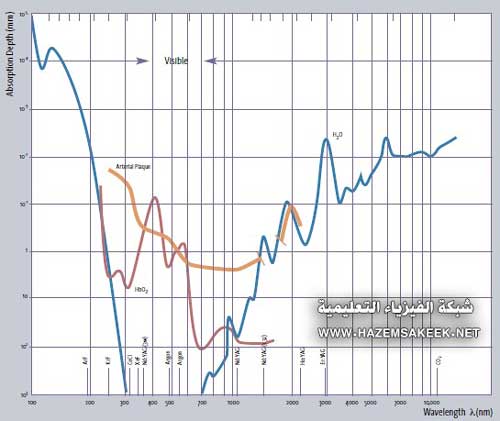
الشكل 2 علاقة عمق الامتصاص مع الطول الموجي
باختيار طول موجي معين ليستخدم في أغشية الأوعية هو عمل واضح إلى حد ما، بمجرد ان يتم تحديد طيف الامتصاص للغشية. في المناطق القريبة من الطيف تحت الأحمر، بين 2000 و 3000 nm، فان الماء هو الأكثر امتصاصا لهذا الطيف، ويكون عمق الاختراق للضوء يتراوح بين 1mm إلى 0.1mm على هذا النطاق من الطيف. وعلى الطرف الأخر من الطيف، في منطقة الفوق بنفسجي بالقرب من 300nm، فان عمق الامتصاص يكون قليل جداً، بسبب الامتصاص بواسطة الجزئيات الخلوية. وعند 308nm، حيث يعمل ليزر الاكسيمر XeCl، حيث ان عمق الامتصاص تقريبا 0.5mm (50mm). الميزة الإضافية لاستخدام الضوء في منطقة الفوق بنفسجية هو قدرته على كسر الروابط الجزيئية مباشرة، بواسطة العملية الفوتوكيميائية. كل فوتون بطول موجي 308nm يحمل طاقة كافية لكسر رابطة كربونية. وتشير القياسات التي أجريت على الأغشية انه حوالي 2% من الفوتونات التي تمتص بواسطة البروتينات واللبيدات في الخلايا تتفكك روابطها، وهذا يضعف تركيب الخلية أو يتسبب في موتها1. هذه الموت المباشر للخلية هو خاصية فريدة تنتج عن تأثير الضوء فوق البنفسجي. الشكل 2 يوضح تأثير الطول الموجي لليزر على عمق الامتصاص.
المتغير التالي في تفاعل الضوء مع الأغشية هو الفترة الزمنية للنبضة pulse width. فلكل أنواع الليزرات، فان طاقة الضوء الممتصة بواسطة الأغشية تتحول إلى حرارة بشكل فوري أو لحظي. ولاستخدام الليزر النبضي، مثل ليزر الاكسيمر XeCl، بشكل ناجح، فان التأثير الحراري يجب ان ينحصر في الأغشية التي يسقط عليها الليزر. هذه هي نبضة الليزر التي يجب ان تعطي طاقتها في فترة زمنية اقل بكثير من الفترة اللازمة لانتشار الحرارة بعيدا عن طرف القسطر2.
عندما نتأكد من حصر التأثير الحراري في منطقة محددة، فان انتزاع ablation بطريقة التبخير المفاجئ للأغشية يمكن ان ينجز من خلال إجبار الأغشية لامتصاص طاقة كافية في نبضة ليزر واحدة لتبخير انفجاري للسائل في الخلايا المائية. هذه العملية تنجز عن طريق نقل طاقة كافية في كل نبضة، من خلال الليفة البصرية للقسطر، وذلك لضمان ان المحتوى المائي في الخلية في منطقة الحصر الحراري تقع تحت نبضة الليزر. باستخدام ليزر الاكسيمر XeCl يتم إضعاف بنية الخلية في البداية عن طريق كسر الروابط بعملية فوتوكيميائية، ومن ثم تنفجر الخلية عندما يتحول المحتوى المائي لها إلى بخار. وهذا يترك بقايا الخلية وحفرة رقيقة تحت القسطر (الشكل 3). هذه البقايا تنتقل بعيدا بدون تفتيت الشعيرات الدموية الطرفية، وبإدخال القسطر بالقرب من الحفرة الناتجة عن نبضة الليزر في الأغشية. وفي النبضة الثانية لليزر، تتكرر العملية، مما يسمح لطرف القسطر بقضم جزء من الأغشية، وكل نبضة ليزر تزيل طبقة رقيقة من الأغشية تحت القسطر. وباستخدام القسطر مع ليزر الاكسيمر XeCl، فان سمك الطبقة المزالة يصل إلى 10mm.

الشكل 3 تكون فقاعات بخارية ضروريا لعملية الانتزاع بالليزر النبضي. تتشكل الفقاعة المؤقتة على كل نبضة ليزر، ويزداد نصف القطر إلى قيمة عظمى تصل إلى 50% اكبر من طرف أنبوب القسطر لمدة 150ms، وتنكمش بالكامل في خلال 100ms عندما يبرد البخار ويتكاثف.
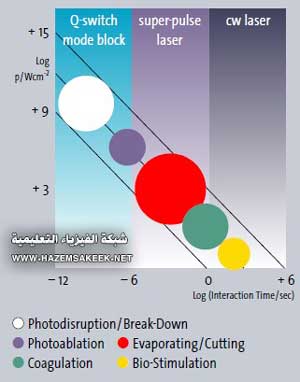
الشكل 4 تأثير طاقة الطول الموجي لليزر بواسطة زمن التفاعل وكثافة الطاقة
أخر متغير في تفاعل ضوء الليزر مع الأغشية هو متوسط الطاقة (الشكل 4). وبشكل مثالي فانه يتطلب استخدام اقل طاقة حرارية تعرض لها الشرايين، حتى لا يحدث أي إصابة حرارية لجدار الشريان تجعله يتشافى بالتكاثر وإعادة الانسداد مرة أخرى. اقل طاقة من نبضة الليزر يمكن ان تحدد بواسطة عمق اختراق الضوء والطاقة اللازمة لإحداث فقاعة بخار في كل نبضة، وهذه تعتبر هي كثافة الطاقة الحركة لكل نوع من انواع الليزر. وفي ليزر الاكسيمر XeCl تكون كثافة الطاقة الحرجة هي 35mJ لكل مليمتر مربع (mJ/mm2) تخرج من طرف الفيبر البصري للقسطر. وليزر الاكسيمر النموذجي بقطر 2mm فان القسطر بمساحة مقطع 0.71mm2 يستطيع توفير طاقة مقدارها 25mJ لكل نبضة. وهذه الطاقة تعتبر كافية لعمل تفاعل قوي مع الأغشية (وهذا مفيد في بعض التطبيقات عندما يكون هناك أغشية صلبة ومتكلسة) ولكن هذا يعطي يولد المزيد من الحرارة.
[divider style=”solid” top=”20″ bottom=”20″]
الليزرات ذات الإشعاع المستمر Continuous Wave Lasers
الليزرات المستخدمة في الطب تم تقييمها لاستخدامها في علاج أكثر الحالات المرضية تعقيدا منذ متوسط الثمانينات من القرن الماضي. والتطبيقات الأولية لاستخدام الليزر في القسطرة لعلاج انسداد وتصلب الشرايين اعتمد على استخدام أشعة الليزر المستمرة (CW)، الذي يولد حرارة عالية عند طرف القسطر ومن الليزرات التي استخدمت في هذا المجال هو ليزر الارجون أو ليزر Nd:YAG.
بالمقارنة مع ليزر الاكسيمر النبضي 308nm مع أنظمة الليزر ذات الإشعاع المستمر فان تلك تحول الطاقة الضوئية إلى طاقة حرارية بصورة مستمرة، ومن ثم تنتشر في الأغشية المصابة والأغشية المحيطة لها. كمية الطاقة الحرارية الكلية المنتقلة من طرف المجس المعدني يتسبب في ارتفاع درجة الحرارة لتصل إلى 450oC (الشكل 5). بالإضافة إلى ذلك فان مجس القسطر يصبح مغطى بطبقة كربونية من احتراق الدم بعد أول تشغيل لليزر. وهذه المشكلة تصبح أكثر وضوحا عندما استخدم ليزر الارجون الذي يعمل عند طول موجي يقع في مدى امتصاص الهيموجلوبين. طبقة الدم الكربونية الناتجة هذه تمتص طاقة الليزر وتمنع التفاعل المباشر بين الليزر والأغشية.

الشكل 5 مجس قسطر ليزر Nd:YAG ذو الإشعاع المستمر
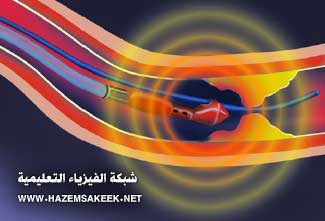
الشكل 6 الطرف الساخن للمجس الناتج عن الليزر المستمر بعد ان تفحم داخل الأوعية
انتزاع الأغشية بواسطة التبخير المفاجئ ablation ينجز عن طريق عملية تعرف باسم denaturation (عملية يفقد فيها البروتين تركيبه نتيجة لتعرضه لإجهاد ما) للخلايا ويتبع بعد دلك بتكربن وتبخل. في حين ان ليزر الإشعاع المستمر يفشل في انتزاع أو اختراق الانسداد المتكلسة. وبالرغم من ارتفاع معدل نجاح هذه التقنية، فان التجارب الأولية التي اعتمدت على التسخين الحراري لليزر ذو الإشعاع المستمر أدت إلى تعقيدات كثيرة مثل تكون aneurysm وهو مرض عصبي، وكذلك حدوث ثقوب في الأوعية وارتفاع معدل الانسداد (الشكل 6)3-7. وكنتيجة لذلك فان أنظمة الليزر ذات الشعاع المتصل تم التخلي عنها في التطبيقات الطبية على الأوعية الدموية.
[divider style=”solid” top=”20″ bottom=”20″]
عمل ليزر الاكسيمر (كلوريد الزينون) (XeCl)
نظرا لاستخدام مصطلح الليزر في كلا من الليزر النبضي والليزر ذو الإشعاع المستمر، فان سلبية استخدام الليزر ذو الإشعاع المستمر صاحبت أيضا نظام ليزر الاكسيمر الحديث، بغض النظر عن الاختلافات الجوهرية بينهما. ومن خلال مراجعة خصائص ليزر الاكسيمر فان هذه النظرة السلبية سوف تزول. ليزر الاكسيمر يستخدم خليط من الغازات كمادة لإنتاج الليزر. احد هذه الغازات يجب ان يكون من الغازات النادرة مثل (Ar، وKr، Xe) والغاز الأخر من الهالوجينات مثل (F أو Cl). الطول الموجي المنبعث من ليزر الاكسيمر يحدد من خلال خليط الغازات المستخدمة فمثلا XeCl يعطي ليزر عند طول موجي 308nm و KrF يعطي ليزر عند 248nm وArF يعطي ليزر عند 193nm إلى أخره. في حالة ليزر XeCl فان غاز Xe وغاز HCl يضافا بكميات بسيطة لغاز النيون الذي يعمل كوسط مساعد. ولكي نجعل الليزر يعطي انبعاث ضوئي فان نبضة كهربية مركزة تعمل تفريغ كهربي للغاز خلال فترة زمنية لا تزيد عن بضعة ns. وفي ليزر الاكسيمر XeCl المستخدم في التطبيقات الطبية فان مقدار الطاقة الكهربية لكل نبضة في حدود 0.3 J وتخرج في صورة ضوء في منطقة الطيف فوق البنفسجي. وباقي الطاقة الكهربية تتحول إلى حرارة مفقودة في داخل الليزر.
عندما يحدث التفريغ الكهربي خلال خليط الغاز المنتج لليزر فان بعض الالكترونات تصطدم مع ذرات الزينون Xe وتتحول إلى ايون موجب Xe+ وتتفكك الجزئيات إلى ذرات هيدروجين وكلور. والمزيد من التصادمات يحول الكلور إلى ايون سالب Cl–. وبمساعدة ذرات النيون فان كلا من ايونات الزينون الموجب وايونات الكلور السالب يتحدان ليشكلا ما يعرف باسم الديمر (وهو عبارة عن ثنائيات من الذرات أو الجزئيات المرتبطة) في مستوى طاقة مثار XeCl*. وعندما يصطدم فوتون ذو طول موجي في منطقة الطيف فوق الأزرق الديمر المثار (الاكسيمر) فان XeCl يحدث انبعاث استحثاثي للتخلص من طاقة الإثارة ويخرج فوتون أخر. وكل جزئ اكسيمر يضيف المزيد من الفوتونات للضوء لتخرج نبضة ليزر. في حين ان الجزئيات الغير مثارة من XeCl تنفصل إلى Xe وCl ويتم إعادة ارتباطهما مرة أخرى تحت تأثير التفريغ الكهربي لنحصل على المزيد من جزئيات XlCl*. وهذه الدورة تكر في اقل من نانوثانية، وتستمر طالما التفريغ الكهربي في غاز الليزر قوي.
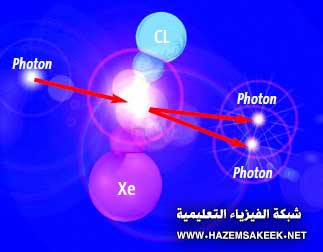
الشكل 7 عملية الإثارة
في حالة ليزر الاكسيمر المستخدم في الطب فان أنبوبة معدنية تحمل خليط غاز XeCl عند ضغط أعلى من الضغط الجوي. وعند فرق جهد عالي مطبق على الأنبوبة المعدنية وعبر خليط الغاز. كما يستخدم كمبيوتر للتحكم في مصدر التغذية الكهربية حسب المدخلات التي يدخلها المستخدم، مثل عدد النبضات في الثانية ومقدار الطاقة لكل نبضة التي سوف تدخل عبر القسطر. ولان القسطر مصنوع من مواد عازلة مثل الكوارتز أو البوليمر، فان الضوء فوق البنفسجي (بدون تيار كهربي أو حرارة) سوف تنتقل عبر القسطر إلى الأنسجة المستهدفة.
[divider style=”solid” top=”20″ bottom=”20″]
أنابيب القسطرة Fiberoptic Catheters
من الطرف النهائي لمركز أنبوب القسطر (حيث يتم إدخال شعاع الليزر فيه) وحتى الطرف الأخر من القسطر (حيث يكون هذا الطرف على اتصال مع الغشاء المتضرر) ويبلغ طول قسطر ليزر الاكسيمر حوالي 3 أمتار. والغلاف الخارجي للقسطر يحيط بكابل من الفيبر البصري، مصنوع من سليكا على درجة عالية من النقاء. والقسطر النموذجي بقطر 2mm يحتوي على ما يقارب 240 ليفة بصرية كل ليفة بصرية بقطر 61mm أي بقطر شعرة إنسان. وعلى نهاية الطرف المتصل بالليزر يتم تركيب حزمة الفايبر بواسطة قطعة توصيل ليدخل شعاع الليزر في داخل الفايبر. ويوصل الفايبر أشعة الليزر إلى الطرف الأخر من القسطر حيث تكون نهاية الفايبر عند طرف القسطر. وعند هذا الطرف فان أنابيب الفايبر البصري ترتب على شكل شبكة أسلاك متلاصقة ومصقولة. خلال عملية الانتزاع بالتبخير المفاجئ للأغشية فان طرفي الفايبر المصقول يكون على اتصال مباشر مع الأغشية المتضررة. ينفذ ضوء الليزر فوق البنفسجي من ألياف الفيبر البصرية وتخترق ما يقارب 50mm من سمك الأغشية وتمتص تلك الأغشية هذه الطاقة الضوئية بشكل مباشر ولا تنحرف هذه الطاقة إلى الجوانب من حول طرف القسطر إنما توجه كل هذه الطاقة إلى المنطقة أسفل طرف القسطر مباشرة.
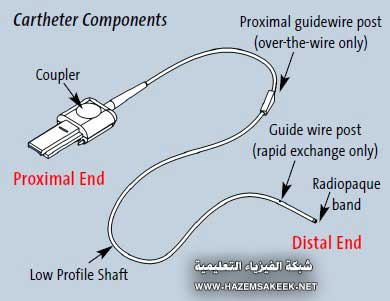
الشكل 8 قسطر ليزر الاكسيمر
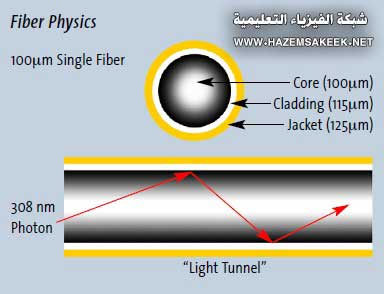
الشكل 9 الحد الفاصل بين القلب والغلاف يعمل كسطح عاكس ليسمح للفوتون بالانتقال خلال حزمة الفيبر البصري

الشكل 10 حزمة ألياف بصرية عند طرفها المتصل بالليزر

الشكل 11 طرف القسطر عند طرفه المتصل مع الأغشية المتضررة.
ليزر الاكسيمر ذو الطول الموجي 308nm يساهم في المعالجة الناجحة لمعظم الحالات الحرجة من خلال انتزاع وإزالة المواد المتخثرة والانسدادات. يعمل الاكسيمر ليزر على إزالة الأورام وتفتيتها لأشكال متعددة للتخلص منها بطريقة أسهل من توسيع الأوعية بطريقة البالون. وعن طريق إزالة بقايا الجلطة فان الليزر يقلل من احتمال حدوث الانسداد على المدى البعيد وكذلك فان الليزر يقلل من إجراء العمليات الجراحية.
[divider style=”solid” top=”20″ bottom=”20″]
مصادر هامة
1. Oraevsky AA, Jacques SL, Pettit GH et al. XeCl laser ablation of atherosclerotic aorta: optical properties and energy pathways. Lasers Surg Med 1992; 12:585-597.
2. Golobic R, Laser Selection Criteria. In Primer on Laser Angioplasty 2nd ed. Ginsberg R, Geschwind HJ, (eds.) Futura Publishing Company Inc, Mount Kisco, 1992.
3. Wollenek G, Laufer G. Comparative study of different laser systems with special regard to angioplasty. Thorac Cardiovasc Surg 1998;36 Suppl 2:126-32.
4. Seeger JM, Kaelin LD. Limitations and pitfalls of laser Surg Annu 1998;36 Pt2:126-32.
5. White RA, White GH, Mehringer MC, Chaing FL, Wilson SE. A clinical trial of laser thermal angioplasty in patients with advanced peripheral vascular disease. Ann Surg 1990 Sep; 212(3):257-65.
6. AbuRahma AF, Robinson PA, Kennard W, Boland JP. Intraoperative perhipheral Nd:YAG laser-assisted thermal balloon angioplasty: short-term and intermeidate-term follow-up. J Vasc Surg 1990 Nov; 12(5):566-72.
7. McAlpin GM, Rama K, Berg RA. Thermal laser assisted balloon angioplasty in lower extremity occlusive disease. Am Surg 1991 Sep;57(9):558-56.